摘要:研究小組發(fā)現(xiàn)了一種以前未知的酶SIRT2。
韓國基礎(chǔ)科學(xué)研究所(IBS)的一個研究團隊發(fā)現(xiàn)了一種之前未知的酶SIRT2,它在與阿爾茨海默病(AD)相關(guān)的記憶喪失中起著關(guān)鍵作用。該研究由IBS認知與社會性研究中心主任李政勛(C Justin LEE)領(lǐng)導(dǎo),為理解星形膠質(zhì)細胞如何通過產(chǎn)生過量的抑制性神經(jīng)遞質(zhì)GABA來促進認知能力下降提供了重要見解。
曾經(jīng)被認為只支持神經(jīng)元的星形膠質(zhì)細胞,現(xiàn)在已知可以積極影響大腦功能。在阿爾茨海默病中,星形膠質(zhì)細胞變得具有反應(yīng)性,這意味著它們會因淀粉樣蛋白β(Aβ)斑塊的存在而改變行為,而淀粉樣蛋白β斑塊是該疾病的標(biāo)志性特征。盡管星形膠質(zhì)細胞試圖清除這些斑塊,但這一過程卻引發(fā)了一系列有害的連鎖反應(yīng)。首先,它們通過自噬作用攝取這些斑塊(Kim和Chun,2024年)并通過尿素循環(huán)將其降解(Ju等,2022年),這是之前研究中發(fā)現(xiàn)的。然而,這種分解導(dǎo)致了GABA的過量產(chǎn)生,從而抑制了大腦活動,導(dǎo)致記憶受損。此外,這一途徑還會產(chǎn)生過氧化氫(H?O?),這是一種有毒副產(chǎn)品,會導(dǎo)致進一步的神經(jīng)元死亡和神經(jīng)退行性病變。
 圖1 SIRT2和ALDH1A1作為阿爾茨海默病星形膠質(zhì)細胞GABA產(chǎn)生的關(guān)鍵酶
圖1 SIRT2和ALDH1A1作為阿爾茨海默病星形膠質(zhì)細胞GABA產(chǎn)生的關(guān)鍵酶IBS研究團隊著手揭示哪些酶負責(zé)過量的GABA產(chǎn)生,希望找到一種方法,能夠在不干擾其他大腦功能的情況下,選擇性地阻斷其有害影響。通過分子分析、顯微鏡成像和電生理學(xué),研究人員確定SIRT2和ALDH1A1是參與阿爾茨海默病受影響的星形膠質(zhì)細胞中GABA過量產(chǎn)生的重要酶。
在常用的AD小鼠模型的星形膠質(zhì)細胞以及死后人類AD患者的大腦中,都發(fā)現(xiàn)SIRT2蛋白有所增加。“當(dāng)我們在AD小鼠中抑制星形膠質(zhì)細胞中SIRT2的表達時,我們觀察到記憶部分恢復(fù),GABA產(chǎn)生減少”,該研究的主要作者、IBS的博士后研究員Mridula BHALLA引用說。“盡管我們預(yù)期GABA釋放會減少,但我們發(fā)現(xiàn)小鼠的短期工作記憶(Y迷宮)得到了恢復(fù),而空間記憶(NPR)卻沒有。這令人興奮,但也給我們留下了更多問題。”
SIRT2參與GABA產(chǎn)生的最后一步,而H?O?則在過程的早期產(chǎn)生。因此,即使在沒有SIRT2的情況下,細胞也可能持續(xù)產(chǎn)生并釋放H?O?。“事實上,我們發(fā)現(xiàn)抑制SIRT2會繼續(xù)產(chǎn)生H?O?,這表明即使GABA產(chǎn)生減少,神經(jīng)退行性病變也可能繼續(xù)”,主任李政勛說。
通過將SIRT2和ALDH1A1確定為下游靶點,科學(xué)家們現(xiàn)在可以有選擇地抑制GABA的產(chǎn)生,而不影響H?O?水平。這是一個關(guān)鍵突破,因為它允許研究人員將GABA和H?O?的影響分開,并研究它們在神經(jīng)退行性病變中的各自作用。
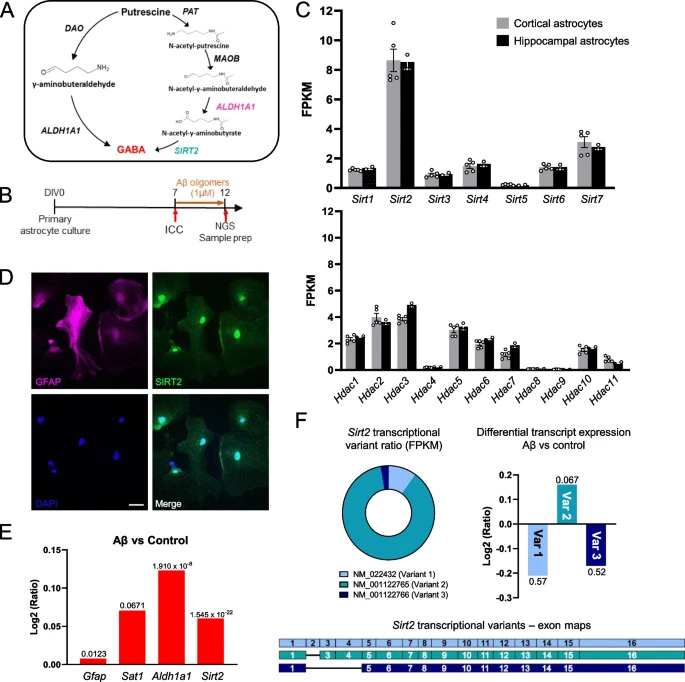
圖2 Sirt2在皮質(zhì)和海馬星形膠質(zhì)細胞中高度表達
主任李政勛強調(diào)了這些發(fā)現(xiàn)的重要性,他說:“到目前為止,我們一直在阿爾茨海默病研究中使用MAOB抑制劑,它阻止了H?O?以及GABA的產(chǎn)生。通過確定MAOB下游的酶SIRT2和ALDH1A1,我們現(xiàn)在可以有選擇地抑制GABA的產(chǎn)生,而不影響H?O?,這將使我們能夠剖析GABA和H?O?的影響,并研究它們在疾病進展中的各自作用。”
盡管SIRT2可能不是直接的藥物靶點,因為其對神經(jīng)退行性病變的影響有限,但這項研究為旨在控制阿爾茨海默病中星形膠質(zhì)細胞反應(yīng)性的更精確治療策略鋪平了道路。
參考資料
[1] SIRT2 and ALDH1A1 as critical enzymes for astrocytic GABA production in Alzheimer’s disease
摘要:研究小組發(fā)現(xiàn)了一種以前未知的酶SIRT2。
韓國基礎(chǔ)科學(xué)研究所(IBS)的一個研究團隊發(fā)現(xiàn)了一種之前未知的酶SIRT2,它在與阿爾茨海默病(AD)相關(guān)的記憶喪失中起著關(guān)鍵作用。該研究由IBS認知與社會性研究中心主任李政勛(C Justin LEE)領(lǐng)導(dǎo),為理解星形膠質(zhì)細胞如何通過產(chǎn)生過量的抑制性神經(jīng)遞質(zhì)GABA來促進認知能力下降提供了重要見解。
曾經(jīng)被認為只支持神經(jīng)元的星形膠質(zhì)細胞,現(xiàn)在已知可以積極影響大腦功能。在阿爾茨海默病中,星形膠質(zhì)細胞變得具有反應(yīng)性,這意味著它們會因淀粉樣蛋白β(Aβ)斑塊的存在而改變行為,而淀粉樣蛋白β斑塊是該疾病的標(biāo)志性特征。盡管星形膠質(zhì)細胞試圖清除這些斑塊,但這一過程卻引發(fā)了一系列有害的連鎖反應(yīng)。首先,它們通過自噬作用攝取這些斑塊(Kim和Chun,2024年)并通過尿素循環(huán)將其降解(Ju等,2022年),這是之前研究中發(fā)現(xiàn)的。然而,這種分解導(dǎo)致了GABA的過量產(chǎn)生,從而抑制了大腦活動,導(dǎo)致記憶受損。此外,這一途徑還會產(chǎn)生過氧化氫(H?O?),這是一種有毒副產(chǎn)品,會導(dǎo)致進一步的神經(jīng)元死亡和神經(jīng)退行性病變。
 圖1 SIRT2和ALDH1A1作為阿爾茨海默病星形膠質(zhì)細胞GABA產(chǎn)生的關(guān)鍵酶
圖1 SIRT2和ALDH1A1作為阿爾茨海默病星形膠質(zhì)細胞GABA產(chǎn)生的關(guān)鍵酶IBS研究團隊著手揭示哪些酶負責(zé)過量的GABA產(chǎn)生,希望找到一種方法,能夠在不干擾其他大腦功能的情況下,選擇性地阻斷其有害影響。通過分子分析、顯微鏡成像和電生理學(xué),研究人員確定SIRT2和ALDH1A1是參與阿爾茨海默病受影響的星形膠質(zhì)細胞中GABA過量產(chǎn)生的重要酶。
在常用的AD小鼠模型的星形膠質(zhì)細胞以及死后人類AD患者的大腦中,都發(fā)現(xiàn)SIRT2蛋白有所增加。“當(dāng)我們在AD小鼠中抑制星形膠質(zhì)細胞中SIRT2的表達時,我們觀察到記憶部分恢復(fù),GABA產(chǎn)生減少”,該研究的主要作者、IBS的博士后研究員Mridula BHALLA引用說。“盡管我們預(yù)期GABA釋放會減少,但我們發(fā)現(xiàn)小鼠的短期工作記憶(Y迷宮)得到了恢復(fù),而空間記憶(NPR)卻沒有。這令人興奮,但也給我們留下了更多問題。”
SIRT2參與GABA產(chǎn)生的最后一步,而H?O?則在過程的早期產(chǎn)生。因此,即使在沒有SIRT2的情況下,細胞也可能持續(xù)產(chǎn)生并釋放H?O?。“事實上,我們發(fā)現(xiàn)抑制SIRT2會繼續(xù)產(chǎn)生H?O?,這表明即使GABA產(chǎn)生減少,神經(jīng)退行性病變也可能繼續(xù)”,主任李政勛說。
通過將SIRT2和ALDH1A1確定為下游靶點,科學(xué)家們現(xiàn)在可以有選擇地抑制GABA的產(chǎn)生,而不影響H?O?水平。這是一個關(guān)鍵突破,因為它允許研究人員將GABA和H?O?的影響分開,并研究它們在神經(jīng)退行性病變中的各自作用。

圖2 Sirt2在皮質(zhì)和海馬星形膠質(zhì)細胞中高度表達
主任李政勛強調(diào)了這些發(fā)現(xiàn)的重要性,他說:“到目前為止,我們一直在阿爾茨海默病研究中使用MAOB抑制劑,它阻止了H?O?以及GABA的產(chǎn)生。通過確定MAOB下游的酶SIRT2和ALDH1A1,我們現(xiàn)在可以有選擇地抑制GABA的產(chǎn)生,而不影響H?O?,這將使我們能夠剖析GABA和H?O?的影響,并研究它們在疾病進展中的各自作用。”
盡管SIRT2可能不是直接的藥物靶點,因為其對神經(jīng)退行性病變的影響有限,但這項研究為旨在控制阿爾茨海默病中星形膠質(zhì)細胞反應(yīng)性的更精確治療策略鋪平了道路。
參考資料
[1] SIRT2 and ALDH1A1 as critical enzymes for astrocytic GABA production in Alzheimer’s disease



