摘要:圣猶大兒童研究醫院的科學家們發現,細胞對低氧的反應也會增加成人胎兒血紅蛋白的表達,這可能會導致一些常見遺傳性貧血的新療法。
圣猶大兒童研究醫院(St. Jude Children’s Research Hospital)的科學家已經展示了一種負責適應低氧環境(缺氧)的蛋白質是如何導致成人胎兒血紅蛋白(HbF)表達增加的。這一發現對治療鐮狀細胞病和乙型地中海貧血有一定的意義,這兩種嚴重的血液疾病影響著數百萬人。這項研究發表在今天的《Nature》。

圖1 研究發現適應低氧環境的蛋白質是如何導致成人胎兒血紅蛋白(HbF)表達增加(圖源:[1])
血紅蛋白就像一塊蛋白質海綿,它能吸收氧氣,并允許紅血球將氧氣運送到全身。成人血紅蛋白包含四個蛋白質亞基-兩個-球蛋白和兩個-球蛋白。球蛋白的突變會導致鐮狀細胞病和-地中海貧血。但是人類有另一種血紅蛋白亞單位基因(γ -球蛋白),它在胎兒發育過程中代替β -球蛋白表達。γ -球蛋白與α -球蛋白結合形成HbF。通常在出生前后,γ -球蛋白的表達被關閉,而β -球蛋白被打開,導致HbF向成人血紅蛋白的轉換。
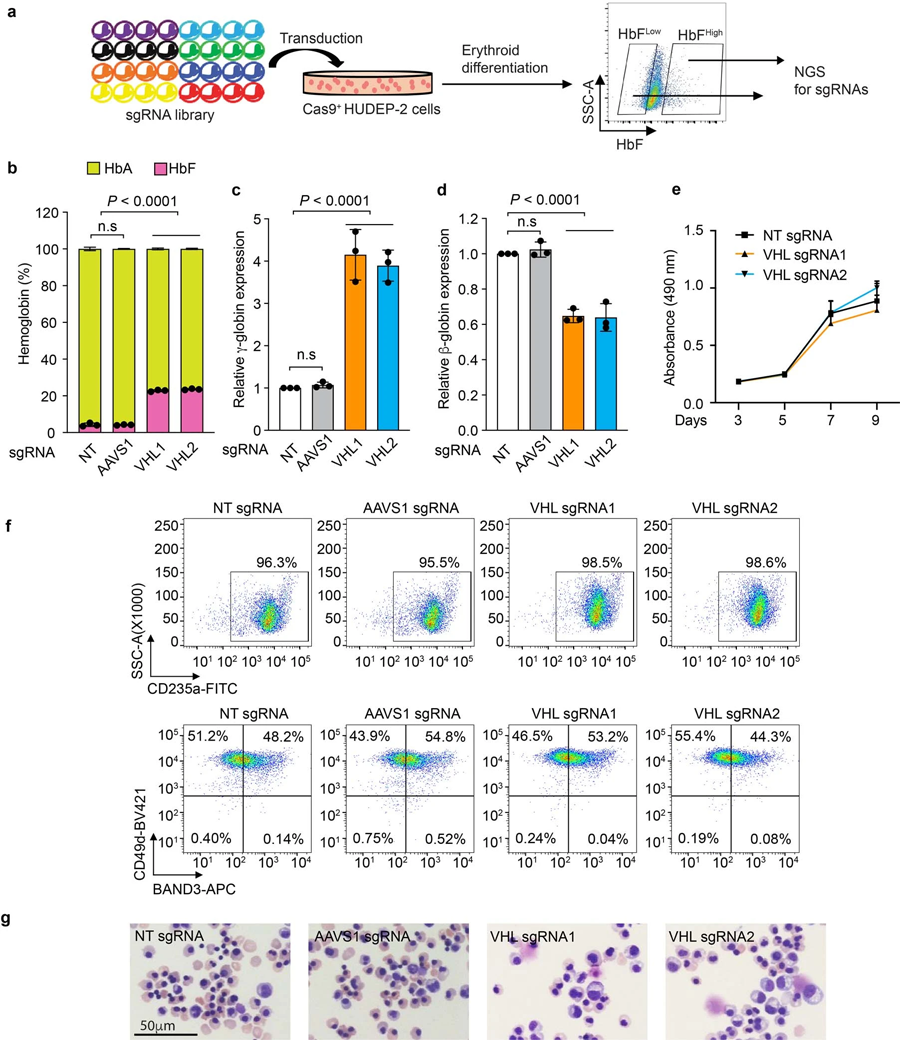
圖2 VHL基因干擾誘導胎兒血紅蛋白(HbF)
“我們多年前就知道,出生后持續表達HbF可以緩解鐮狀細胞病和-地中海貧血的癥狀,”通訊作者Mitchell J. Weiss博士說,他是圣猶大血液科主任。“非常高的HbF水平可以治愈這些疾病,盡管存在缺陷的-球蛋白基因。因此,許多實驗室都專注于了解圍產期從γ -球蛋白基因表達到β -球蛋白基因表達的轉變,并找出用藥物或基因療法逆轉這一轉變的新方法。”

圖3 通訊作者Mitchell J Weiss醫學博士,圣猶大血液科主任醫師;第一作者Ruopeng Feng,圣猶大血液科博士
恢復成人HbF的產生
圣猶大研究小組發現,缺氧誘導因子1 (HIF1)直接促進γ -球蛋白基因的轉錄,以增強HbF的產生。HIF1是細胞感知和適應缺氧條件能力的重要組成部分。在低氧條件下,HIF1在許多組織中聚集并激活數百個基因,包括紅細胞中的HbF。
第一作者Ruopeng Feng博士是Weiss實驗室的一名科學家,他證明了一種可以激活部分細胞缺氧反應的藥物可以抑制來自鐮狀細胞病成人的紅細胞的鐮狀化。這種藥物是一種脯氨酸羥化酶抑制劑,它導致HIF1積累,結合γ-球蛋白基因附近的DNA調控區,激活其轉錄產生HbF,抑制細胞鐮狀細胞。脯氨酸羥化酶抑制劑目前正處于治療慢性腎臟疾病相關貧血的晚期臨床研發階段。這些藥物通過穩定HIF蛋白來刺激促紅細胞生成素的產生,促紅細胞生成素是一種促進紅細胞產生的激素。
Weiss說:“我們的研究結果表明,脯氨酸羥化酶抑制劑可能對治療鐮狀細胞病或乙型地中海貧血有用,在這些疾病中,啟動HbF產生具有治療效益。大約20%的成年鐮狀細胞病患者會出現腎衰竭和相關貧血。脯氨酸羥化酶抑制劑可能對這些人有雙重作用,通過刺激促紅細胞生成素和HbF的產生。”
將缺氧反應與HbF聯系起來
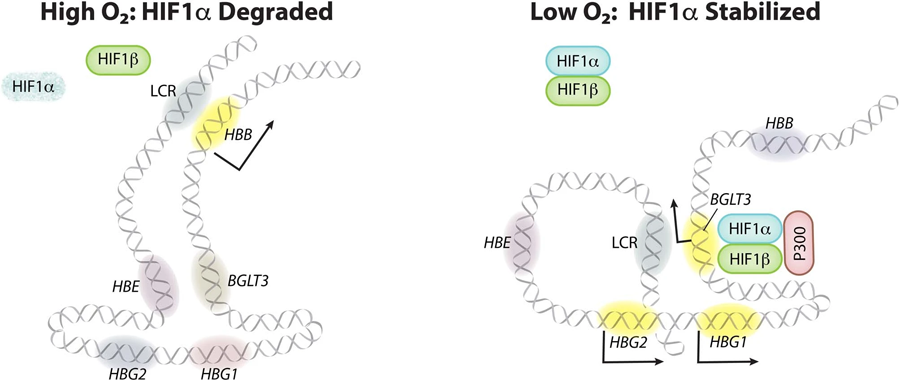
圖4 成人型紅細胞中HIF1α激活γ-珠蛋白轉錄的模型(HbF)
2019年,諾貝爾生理學或醫學獎授予了HIF通路的發現。目前,由Weiss團隊領導的研究建立了這種缺氧適應和HbF表達之間的直接聯系。這種聯系解釋了長期以來的臨床觀察,即HbF是在暴露于缺氧或某些形式的貧血(稱為“應激性紅細胞生成”)后紅細胞加速生成過程中誘導的。
Weiss說:“球蛋白作為HIF靶基因的鑒定支持了HbF進化為一種對抗缺氧的保護機制的概念。對血紅蛋白50多年的研究確立了生物學和醫學上的許多普遍原則。對血紅蛋白和球蛋白基因表達的研究不斷產生新的臨床相關發現,這是令人興奮和欣慰的。”
參考資料:
[1] Activation of γ-globin expression by hypoxia-inducible factor 1α
摘要:圣猶大兒童研究醫院的科學家們發現,細胞對低氧的反應也會增加成人胎兒血紅蛋白的表達,這可能會導致一些常見遺傳性貧血的新療法。
圣猶大兒童研究醫院(St. Jude Children’s Research Hospital)的科學家已經展示了一種負責適應低氧環境(缺氧)的蛋白質是如何導致成人胎兒血紅蛋白(HbF)表達增加的。這一發現對治療鐮狀細胞病和乙型地中海貧血有一定的意義,這兩種嚴重的血液疾病影響著數百萬人。這項研究發表在今天的《Nature》。

圖1 研究發現適應低氧環境的蛋白質是如何導致成人胎兒血紅蛋白(HbF)表達增加(圖源:[1])
血紅蛋白就像一塊蛋白質海綿,它能吸收氧氣,并允許紅血球將氧氣運送到全身。成人血紅蛋白包含四個蛋白質亞基-兩個-球蛋白和兩個-球蛋白。球蛋白的突變會導致鐮狀細胞病和-地中海貧血。但是人類有另一種血紅蛋白亞單位基因(γ -球蛋白),它在胎兒發育過程中代替β -球蛋白表達。γ -球蛋白與α -球蛋白結合形成HbF。通常在出生前后,γ -球蛋白的表達被關閉,而β -球蛋白被打開,導致HbF向成人血紅蛋白的轉換。

圖2 VHL基因干擾誘導胎兒血紅蛋白(HbF)
“我們多年前就知道,出生后持續表達HbF可以緩解鐮狀細胞病和-地中海貧血的癥狀,”通訊作者Mitchell J. Weiss博士說,他是圣猶大血液科主任。“非常高的HbF水平可以治愈這些疾病,盡管存在缺陷的-球蛋白基因。因此,許多實驗室都專注于了解圍產期從γ -球蛋白基因表達到β -球蛋白基因表達的轉變,并找出用藥物或基因療法逆轉這一轉變的新方法。”

圖3 通訊作者Mitchell J Weiss醫學博士,圣猶大血液科主任醫師;第一作者Ruopeng Feng,圣猶大血液科博士
恢復成人HbF的產生
圣猶大研究小組發現,缺氧誘導因子1 (HIF1)直接促進γ -球蛋白基因的轉錄,以增強HbF的產生。HIF1是細胞感知和適應缺氧條件能力的重要組成部分。在低氧條件下,HIF1在許多組織中聚集并激活數百個基因,包括紅細胞中的HbF。
第一作者Ruopeng Feng博士是Weiss實驗室的一名科學家,他證明了一種可以激活部分細胞缺氧反應的藥物可以抑制來自鐮狀細胞病成人的紅細胞的鐮狀化。這種藥物是一種脯氨酸羥化酶抑制劑,它導致HIF1積累,結合γ-球蛋白基因附近的DNA調控區,激活其轉錄產生HbF,抑制細胞鐮狀細胞。脯氨酸羥化酶抑制劑目前正處于治療慢性腎臟疾病相關貧血的晚期臨床研發階段。這些藥物通過穩定HIF蛋白來刺激促紅細胞生成素的產生,促紅細胞生成素是一種促進紅細胞產生的激素。
Weiss說:“我們的研究結果表明,脯氨酸羥化酶抑制劑可能對治療鐮狀細胞病或乙型地中海貧血有用,在這些疾病中,啟動HbF產生具有治療效益。大約20%的成年鐮狀細胞病患者會出現腎衰竭和相關貧血。脯氨酸羥化酶抑制劑可能對這些人有雙重作用,通過刺激促紅細胞生成素和HbF的產生。”
將缺氧反應與HbF聯系起來

圖4 成人型紅細胞中HIF1α激活γ-珠蛋白轉錄的模型(HbF)
2019年,諾貝爾生理學或醫學獎授予了HIF通路的發現。目前,由Weiss團隊領導的研究建立了這種缺氧適應和HbF表達之間的直接聯系。這種聯系解釋了長期以來的臨床觀察,即HbF是在暴露于缺氧或某些形式的貧血(稱為“應激性紅細胞生成”)后紅細胞加速生成過程中誘導的。
Weiss說:“球蛋白作為HIF靶基因的鑒定支持了HbF進化為一種對抗缺氧的保護機制的概念。對血紅蛋白50多年的研究確立了生物學和醫學上的許多普遍原則。對血紅蛋白和球蛋白基因表達的研究不斷產生新的臨床相關發現,這是令人興奮和欣慰的。”
參考資料:
[1] Activation of γ-globin expression by hypoxia-inducible factor 1α



