摘要:美國國家過敏和傳染病研究所(NIAID)和沃爾特?里德陸軍研究所領導的研究團隊近日針對EB病毒的不同位點,開發出一組研究性的單克隆抗體(mAb)。
美國國家過敏和傳染病研究所(NIAID)和沃爾特?里德陸軍研究所領導的研究團隊近日針對EB病毒的不同位點,開發出一組研究性的單克隆抗體(mAb)。
在實驗室環境中對人類細胞進行測試時,它們阻斷了感染。此外,在對小鼠進行測試時,其中一種研究性單克隆抗體對EB病毒感染和淋巴瘤形成提供了幾乎完全的保護。這項研究結果于10月27日發表在《Immunity》雜志上。

圖1 研究人員針對EB病毒的不同位點開發出一組研究性的單克隆抗體
EB病毒是最常見的人類病毒之一。EB病毒感染后,病毒在體內處于休眠狀態,但在某些情況下可能會重新激活。它會引起傳染性單核細胞增多癥,并與某些癌癥(包括霍奇金淋巴瘤和鼻咽癌)和自身免疫性疾病(如多發性硬化癥)有關。
一些免疫力較弱的人,比如移植受者,更容易在EB病毒感染后出現嚴重的癥狀和并發癥。目前還沒有疫苗獲得批準,來預防這種病毒。
研究人員針對EB病毒表面的兩種關鍵蛋白質(gH和gL)開發出研究性單克隆抗體。目前已知這兩種蛋白質可促進EB病毒與人類細胞的融合,并引起感染。在實驗室環境下進行測試時,研究性單克隆抗體防止了人類B細胞和上皮細胞的EB病毒感染,這些細胞位于病毒感染的初始部位。
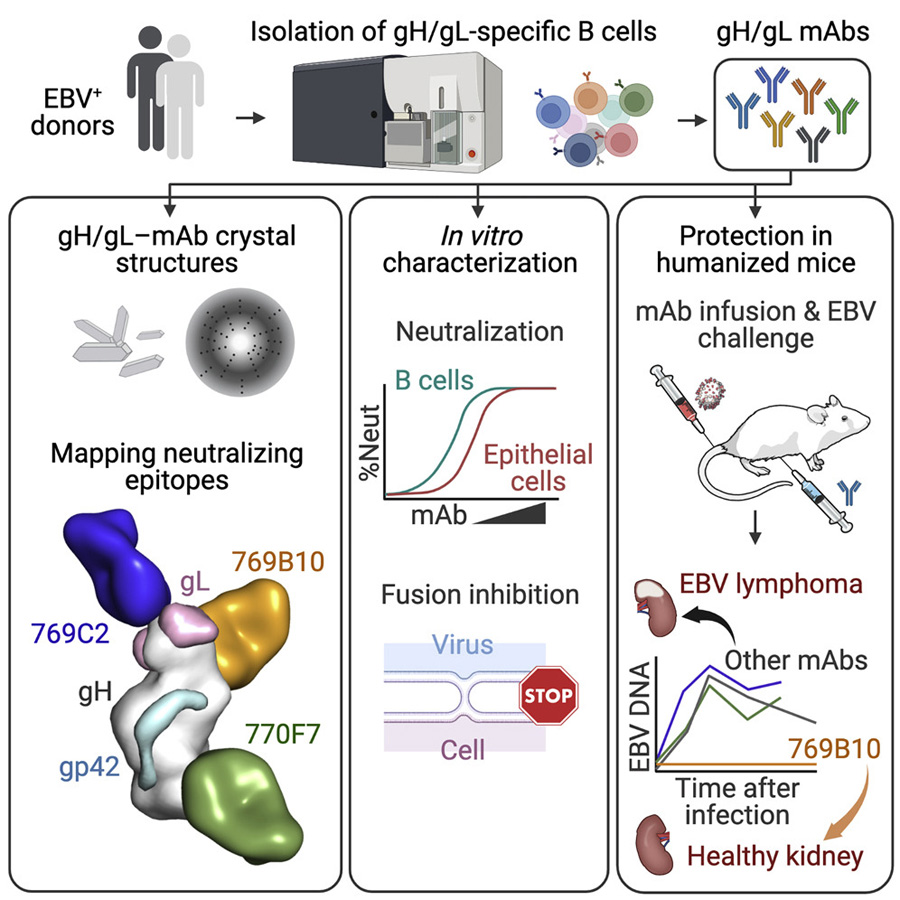
圖2 針對EB病毒表面的兩種關鍵蛋白質(gH和gL)開發出研究性單克隆抗體
他們又通過X射線晶體衍射和顯微鏡來分析單克隆抗體和兩種表面蛋白的結構,確定了病毒上多個易受攻擊的部位。在小鼠身上進行測試時,一種名為mAb 769B10的研究性單克隆抗體對EB病毒感染提供了幾乎完全的保護。這種單克隆抗體還能防止所有測試的小鼠患上與EB病毒有關的淋巴瘤。
研究人員稱,這些發現強調了可行的EB病毒疫苗靶點以及單獨使用或聯合使用研究性單克隆抗體的潛力,有望預防或治療免疫缺陷患者的EB病毒感染。作者指出,他們還計劃針對mAb 769B10開展更多的研究。
參考資料:
[1] WH Chen et al. Epstein-Barr virus gH/gL has multiple sites of vulnerability for virus neutralization and fusion inhibition. Immunity DOI: 10.1016/j.immuni.2022.10.003 (2022).
摘要:美國國家過敏和傳染病研究所(NIAID)和沃爾特?里德陸軍研究所領導的研究團隊近日針對EB病毒的不同位點,開發出一組研究性的單克隆抗體(mAb)。
美國國家過敏和傳染病研究所(NIAID)和沃爾特?里德陸軍研究所領導的研究團隊近日針對EB病毒的不同位點,開發出一組研究性的單克隆抗體(mAb)。
在實驗室環境中對人類細胞進行測試時,它們阻斷了感染。此外,在對小鼠進行測試時,其中一種研究性單克隆抗體對EB病毒感染和淋巴瘤形成提供了幾乎完全的保護。這項研究結果于10月27日發表在《Immunity》雜志上。

圖1 研究人員針對EB病毒的不同位點開發出一組研究性的單克隆抗體
EB病毒是最常見的人類病毒之一。EB病毒感染后,病毒在體內處于休眠狀態,但在某些情況下可能會重新激活。它會引起傳染性單核細胞增多癥,并與某些癌癥(包括霍奇金淋巴瘤和鼻咽癌)和自身免疫性疾病(如多發性硬化癥)有關。
一些免疫力較弱的人,比如移植受者,更容易在EB病毒感染后出現嚴重的癥狀和并發癥。目前還沒有疫苗獲得批準,來預防這種病毒。
研究人員針對EB病毒表面的兩種關鍵蛋白質(gH和gL)開發出研究性單克隆抗體。目前已知這兩種蛋白質可促進EB病毒與人類細胞的融合,并引起感染。在實驗室環境下進行測試時,研究性單克隆抗體防止了人類B細胞和上皮細胞的EB病毒感染,這些細胞位于病毒感染的初始部位。

圖2 針對EB病毒表面的兩種關鍵蛋白質(gH和gL)開發出研究性單克隆抗體
他們又通過X射線晶體衍射和顯微鏡來分析單克隆抗體和兩種表面蛋白的結構,確定了病毒上多個易受攻擊的部位。在小鼠身上進行測試時,一種名為mAb 769B10的研究性單克隆抗體對EB病毒感染提供了幾乎完全的保護。這種單克隆抗體還能防止所有測試的小鼠患上與EB病毒有關的淋巴瘤。
研究人員稱,這些發現強調了可行的EB病毒疫苗靶點以及單獨使用或聯合使用研究性單克隆抗體的潛力,有望預防或治療免疫缺陷患者的EB病毒感染。作者指出,他們還計劃針對mAb 769B10開展更多的研究。
參考資料:
[1] WH Chen et al. Epstein-Barr virus gH/gL has multiple sites of vulnerability for virus neutralization and fusion inhibition. Immunity DOI: 10.1016/j.immuni.2022.10.003 (2022).



