摘要:如果B細胞是免疫系統的兵工廠,制造抗體來中和有害的病原體,那么被稱為生發中心的微小生物結構就是它的武器開發設施。
如果B細胞是免疫系統的兵工廠,制造抗體來中和有害病原體,那么被稱為生發中心的微小生物結構就是它的武器開發設施。這些微小的訓練場是為了應對感染和接種疫苗而形成的,可以讓B細胞完善它們針對特定病毒和細菌部署的抗體。
因此,弄清楚生發中心是如何工作的對于理解免疫和開發更有效的疫苗至關重要。現在,《Cell》雜志上的一項新研究揭示了為什么一些生發中心可以持續幾個月而不是幾周,為未來的疫苗設計提供了見解。

圖1 新研究揭示了生發中心是如何工作的(圖源:[1])
舊瓶裝新酒
生發中心在接種疫苗或感染后不久在身體的淋巴組織中形成。一旦進入生發中心,B細胞就會發生快速突變,通過自然選擇的過程,只有帶有抗體的B細胞才能最有效地與目標抗原結合。然后,這些高級B細胞要么變成漿細胞,即分泌大量抗體進入血清的抗體工廠,要么變成記憶B細胞,在體內巡邏,尋找它們進化來對抗的病原體回歸的跡象。
洛克菲勒大學Gabriel D. Victoria實驗室的博士后Renan V.H. de Carvalho說:“生發中心的目標是產生高親和力的漿細胞和記憶B細胞,然后輸出。”
在小鼠中,大多數生發中心在完成生產高親和力B細胞的目標后幾周后關閉。但那些為應對某些呼吸道感染(包括流感)而形成的病毒,可以持續六個多月,大約是一只小鼠正常壽命的四分之一。De Carvalho和他的同事們想要了解為什么這些生發中心如此長壽,以及它們內部到底發生了什么。
在這項研究中,研究人員首先用流感病毒和SARS-CoV-2病毒感染小鼠,等待它們形成生發中心,然后在24周內對從這些中心收獲的B細胞的抗體基因進行測序。令他們驚訝的是,他們發現抗體優化并沒有以穩定的速度持續進化,而是在12周后達到頂峰,然后明顯退化,即使該中心仍然活躍。研究人員后來發現,這種令人費解的下降是由于不斷將未進化的“幼稚”B細胞引入生發中心。
隨著幾周變成幾個月,一個更完整的圖景開始形成:最初為長壽生發中心播下種子的創始B細胞逐漸被幼稚細胞所取代,因此,只有一小部分晚期生發中心是由啟動它們的B細胞的后代組成的。
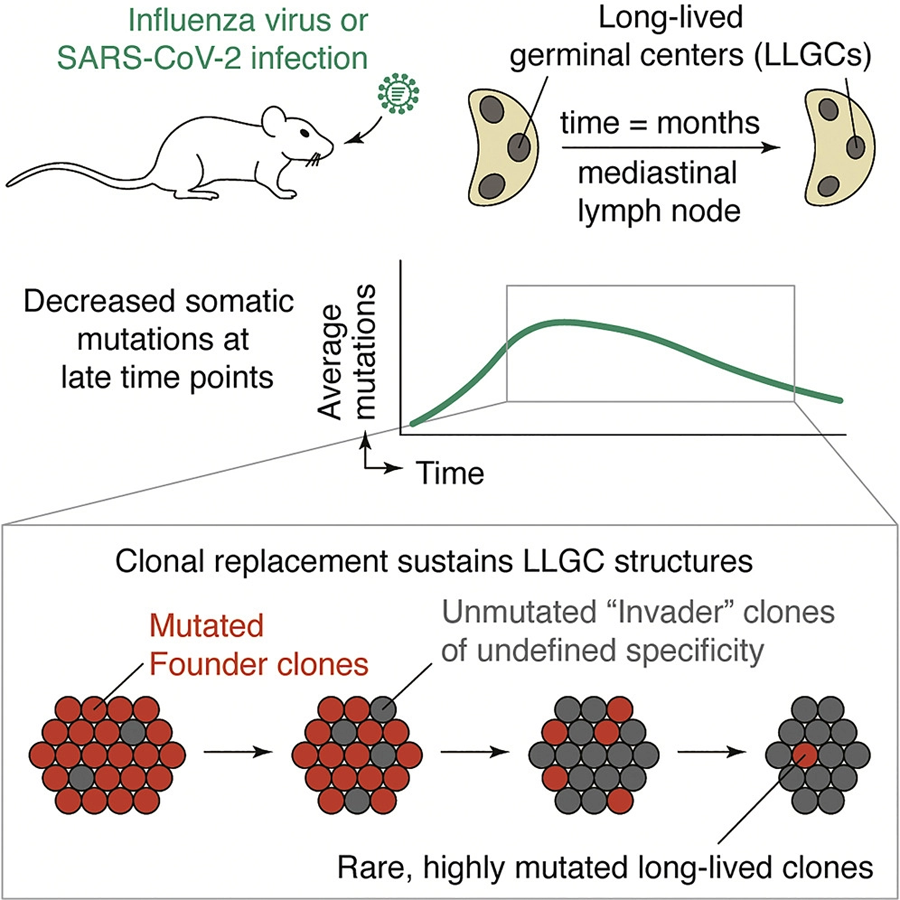
圖2 研究人員用流感病毒和SARS-CoV-2病毒感染小鼠,對B細胞的抗體基因進行測序(圖源:[1])
老派和新派
這些新加入的B細胞與生發中心的原始B細胞不同。隨后的實驗表明,雖然幼稚 B細胞也在生發中心內發生了進化,但它們沒有產生可以與流感或SARS-CoV2抗原結合的抗體。
“我們過去認為感染誘導的生發中心是針對特定病原體抗原的單一反應,”de Carvalho說。“顯然不是,至少在這些長壽的生發中心的情況下是這樣。”
但留在原處的少數原始B細胞足以對最初的病原體產生有效的免疫。當研究人員在小鼠首次感染流感抗原3個月后(有效地模擬重復感染或加強注射)再次將小鼠暴露于流感抗原時,他們證明了許多開始產生抗體的記憶B細胞來自于少數在生發中心逗留了數月的創始細胞,而不是它們的幼稚替代品。
de Carvalho說:“盡管它們只占后來細胞總數的一小部分,但在生發中心停留很長一段時間的創始細胞仍在發揮作用。”但是,這些創始B細胞的工作表現如何,以及幼稚新招募的B細胞是否會限制它們的風格并降低它們的功效,仍有待觀察。Victoria實驗室未來的研究將解決這個問題。
與此同時,這些發現已經對我們對生發中心如何運作的一般理解產生了影響。了解創始人B細胞和幼稚 B細胞之間的動態可以幫助研究人員利用長壽的生發中心產生更有效的抗體來對抗危險的呼吸道病毒,如流感和SARS-CoV-2。
“B細胞連續波對生發中心結構的入侵可能會成為預測生發中心結果的一個重要因素,可能遠遠超出這個特定的流感模型,”Victoria說,“并且可能會給我們一些關于如何誘導生發中心產生我們需要的抗體的見解。”
參考資料:
[1] Clonal replacement sustains long-lived germinal centers primed by respiratory viruses
摘要:如果B細胞是免疫系統的兵工廠,制造抗體來中和有害的病原體,那么被稱為生發中心的微小生物結構就是它的武器開發設施。
如果B細胞是免疫系統的兵工廠,制造抗體來中和有害病原體,那么被稱為生發中心的微小生物結構就是它的武器開發設施。這些微小的訓練場是為了應對感染和接種疫苗而形成的,可以讓B細胞完善它們針對特定病毒和細菌部署的抗體。
因此,弄清楚生發中心是如何工作的對于理解免疫和開發更有效的疫苗至關重要。現在,《Cell》雜志上的一項新研究揭示了為什么一些生發中心可以持續幾個月而不是幾周,為未來的疫苗設計提供了見解。

圖1 新研究揭示了生發中心是如何工作的(圖源:[1])
舊瓶裝新酒
生發中心在接種疫苗或感染后不久在身體的淋巴組織中形成。一旦進入生發中心,B細胞就會發生快速突變,通過自然選擇的過程,只有帶有抗體的B細胞才能最有效地與目標抗原結合。然后,這些高級B細胞要么變成漿細胞,即分泌大量抗體進入血清的抗體工廠,要么變成記憶B細胞,在體內巡邏,尋找它們進化來對抗的病原體回歸的跡象。
洛克菲勒大學Gabriel D. Victoria實驗室的博士后Renan V.H. de Carvalho說:“生發中心的目標是產生高親和力的漿細胞和記憶B細胞,然后輸出。”
在小鼠中,大多數生發中心在完成生產高親和力B細胞的目標后幾周后關閉。但那些為應對某些呼吸道感染(包括流感)而形成的病毒,可以持續六個多月,大約是一只小鼠正常壽命的四分之一。De Carvalho和他的同事們想要了解為什么這些生發中心如此長壽,以及它們內部到底發生了什么。
在這項研究中,研究人員首先用流感病毒和SARS-CoV-2病毒感染小鼠,等待它們形成生發中心,然后在24周內對從這些中心收獲的B細胞的抗體基因進行測序。令他們驚訝的是,他們發現抗體優化并沒有以穩定的速度持續進化,而是在12周后達到頂峰,然后明顯退化,即使該中心仍然活躍。研究人員后來發現,這種令人費解的下降是由于不斷將未進化的“幼稚”B細胞引入生發中心。
隨著幾周變成幾個月,一個更完整的圖景開始形成:最初為長壽生發中心播下種子的創始B細胞逐漸被幼稚細胞所取代,因此,只有一小部分晚期生發中心是由啟動它們的B細胞的后代組成的。

圖2 研究人員用流感病毒和SARS-CoV-2病毒感染小鼠,對B細胞的抗體基因進行測序(圖源:[1])
老派和新派
這些新加入的B細胞與生發中心的原始B細胞不同。隨后的實驗表明,雖然幼稚 B細胞也在生發中心內發生了進化,但它們沒有產生可以與流感或SARS-CoV2抗原結合的抗體。
“我們過去認為感染誘導的生發中心是針對特定病原體抗原的單一反應,”de Carvalho說。“顯然不是,至少在這些長壽的生發中心的情況下是這樣。”
但留在原處的少數原始B細胞足以對最初的病原體產生有效的免疫。當研究人員在小鼠首次感染流感抗原3個月后(有效地模擬重復感染或加強注射)再次將小鼠暴露于流感抗原時,他們證明了許多開始產生抗體的記憶B細胞來自于少數在生發中心逗留了數月的創始細胞,而不是它們的幼稚替代品。
de Carvalho說:“盡管它們只占后來細胞總數的一小部分,但在生發中心停留很長一段時間的創始細胞仍在發揮作用。”但是,這些創始B細胞的工作表現如何,以及幼稚新招募的B細胞是否會限制它們的風格并降低它們的功效,仍有待觀察。Victoria實驗室未來的研究將解決這個問題。
與此同時,這些發現已經對我們對生發中心如何運作的一般理解產生了影響。了解創始人B細胞和幼稚 B細胞之間的動態可以幫助研究人員利用長壽的生發中心產生更有效的抗體來對抗危險的呼吸道病毒,如流感和SARS-CoV-2。
“B細胞連續波對生發中心結構的入侵可能會成為預測生發中心結果的一個重要因素,可能遠遠超出這個特定的流感模型,”Victoria說,“并且可能會給我們一些關于如何誘導生發中心產生我們需要的抗體的見解。”
參考資料:
[1] Clonal replacement sustains long-lived germinal centers primed by respiratory viruses



