摘要:卡羅林斯卡學(xué)院的研究人員發(fā)現(xiàn),編碼T細(xì)胞受體的基因在人和人群之間存在很大差異,這可能解釋了為什么我們對(duì)感染等疾病的反應(yīng)不同。發(fā)表在《免疫》雜志上的研究結(jié)果還表明,一些基因變異遺傳自尼安德特人。
卡羅林斯卡學(xué)院的研究人員發(fā)現(xiàn),編碼T細(xì)胞受體的基因在人和人群之間存在很大差異,這可能解釋了為什么我們對(duì)感染等疾病的反應(yīng)不同。發(fā)表在《免疫》雜志上的研究結(jié)果還表明,一些基因變異遺傳自尼安德特人。
T細(xì)胞是我們免疫系統(tǒng)的一部分,在預(yù)防感染和癌癥方面起著核心作用。在TCRs的幫助下,這些細(xì)胞識(shí)別外來(lái)入侵者和腫瘤細(xì)胞。

圖1 研究人員發(fā)現(xiàn)編碼T細(xì)胞受體的基因在人和人群之間存在很大差異(圖源:[1])
該研究的主要作者Gunilla Karlsson Hedestam說(shuō):“人類TCR基因的變化程度以前是未知的。”
通過(guò)對(duì)血液樣本的深度測(cè)序,研究人員檢測(cè)了來(lái)自撒哈拉以南非洲、東亞、南亞和歐洲的45人的TCR基因。研究人員表明,這些基因在不同的人和人群之間差異很大。這一結(jié)果得到了1000個(gè)基因組計(jì)劃中數(shù)千個(gè)額外病例的分析的證實(shí)。
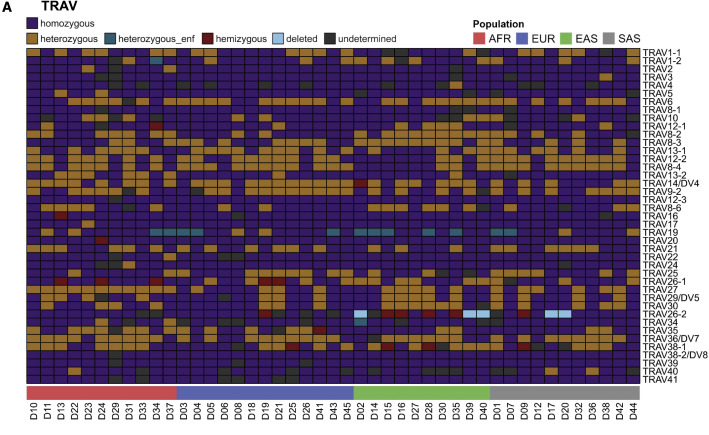
圖2 45名供體的TRAV基因量
“我們發(fā)現(xiàn),除了同卵雙胞胎,每個(gè)人都有一組獨(dú)特的TCR基因變異。這些差異揭示了我們?cè)谌巳核缴嫌^察到的對(duì)感染和疫苗的廣泛反應(yīng)的可能機(jī)制”。
“我們發(fā)現(xiàn)了175個(gè)新的基因變異,這是已知TCR基因變異數(shù)量的兩倍。一個(gè)意想不到和令人驚訝的發(fā)現(xiàn)是,某些基因變異起源于尼安德特人,其中一種存在于歐洲和亞洲20%的現(xiàn)代人身上。”
Gunilla Karlsson Hedestam解釋說(shuō),這些基因的變異無(wú)法用全基因組測(cè)序中使用的標(biāo)準(zhǔn)方法檢測(cè)到,但隨著專門的深度測(cè)序方法和分析軟件的發(fā)展,可以高度精確地定義B細(xì)胞和t細(xì)胞受體基因,這現(xiàn)在是可能的。
Martin Corcoran說(shuō):“由于這些基因是我們基因組中最易變的基因之一,研究結(jié)果也為我們的免疫系統(tǒng)在歷史進(jìn)程中是如何發(fā)展的提供了新的信息。”我們特別感興趣的是揭示我們從尼安德特人祖先那里遺傳的TCR變體的功能。這些變異在現(xiàn)代人身上的頻率表明,在我們的生物學(xué)中有一種有利的功能,我們渴望了解這一點(diǎn),”馬丁·科克倫補(bǔ)充道。
研究人員現(xiàn)在發(fā)表的這些發(fā)現(xiàn)和新的TCR基因數(shù)據(jù)庫(kù)對(duì)未來(lái)新的治療方法的發(fā)展具有重要意義。
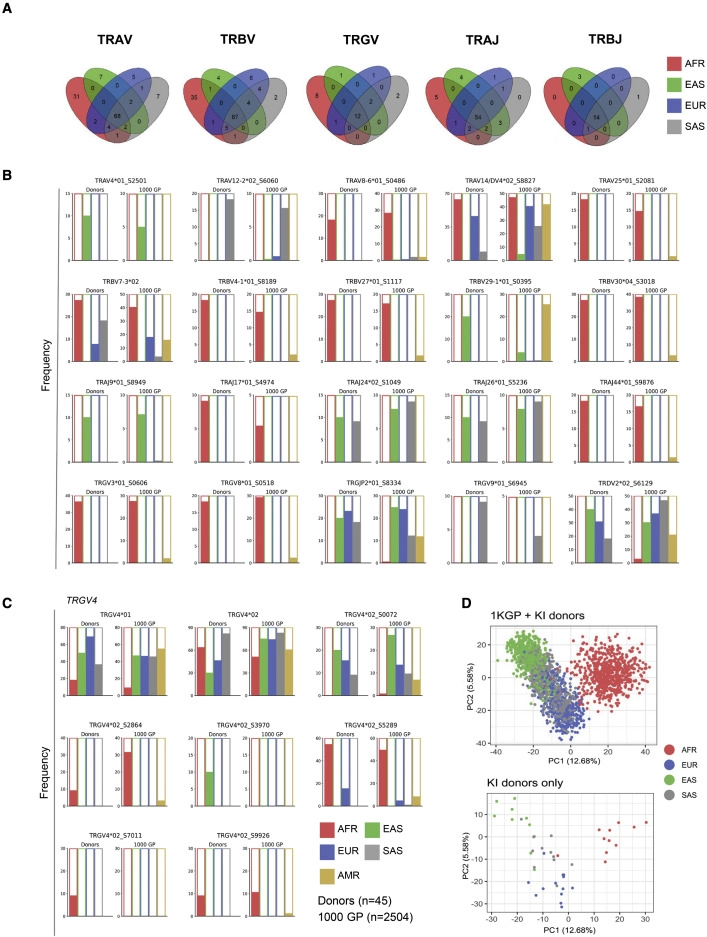
圖3 TCR等位基因的群體差異(圖源:[1])
“了解人類遺傳學(xué)是開發(fā)靶向治療的基礎(chǔ)。研究中描述的方法提供了新的機(jī)會(huì),尤其是在癌癥領(lǐng)域,t細(xì)胞是幾種有前途的免疫治療形式的核心。”Gunilla Karlsson Hedestam說(shuō)。
研究結(jié)果還可以為其他領(lǐng)域的研究提供啟示。
Gunilla Karlsson Hedestam說(shuō):“這些發(fā)現(xiàn)可能導(dǎo)致包括精準(zhǔn)醫(yī)學(xué)在內(nèi)的一系列醫(yī)學(xué)學(xué)科開發(fā)新的診斷和治療方法。”
“我們現(xiàn)在正在研究幾個(gè)新發(fā)現(xiàn)的基因變異的功能意義,以及這種變異如何影響我們的t細(xì)胞反應(yīng)。我們還計(jì)劃進(jìn)行大規(guī)模的個(gè)體研究,以研究TCR基因變異在我們已知的涉及T細(xì)胞的疾病中所起的作用,如傳染病、癌癥和自身免疫性疾病,”Gunilla Karlsson Hedestam說(shuō)。
這些實(shí)驗(yàn)是在麥考瑞Galleria研究機(jī)構(gòu)使用道德的Galleria mellonella(大蠟蛾幼蟲)動(dòng)物模型替代進(jìn)行的,這是澳大利亞第一個(gè)這樣的動(dòng)物模型。
參考資料:
[1] Archaic humans have contributed to large-scale variation in modern human T cell receptor genes. Martin Corcoran, Mark Chernyshev, Marco Mandolesi, Sanjana Narang, Mateusz Kaduk, Kewei Ye, Christopher Sundling, Anna F?rnert, Taras Kreslavsky, Carolina Bernhardsson, Maximilian Larena, Mattias Jakobsson, Gunilla B. Karlsson Hedestam, Immunity, online den 15 februari 2023.
摘要:卡羅林斯卡學(xué)院的研究人員發(fā)現(xiàn),編碼T細(xì)胞受體的基因在人和人群之間存在很大差異,這可能解釋了為什么我們對(duì)感染等疾病的反應(yīng)不同。發(fā)表在《免疫》雜志上的研究結(jié)果還表明,一些基因變異遺傳自尼安德特人。
卡羅林斯卡學(xué)院的研究人員發(fā)現(xiàn),編碼T細(xì)胞受體的基因在人和人群之間存在很大差異,這可能解釋了為什么我們對(duì)感染等疾病的反應(yīng)不同。發(fā)表在《免疫》雜志上的研究結(jié)果還表明,一些基因變異遺傳自尼安德特人。
T細(xì)胞是我們免疫系統(tǒng)的一部分,在預(yù)防感染和癌癥方面起著核心作用。在TCRs的幫助下,這些細(xì)胞識(shí)別外來(lái)入侵者和腫瘤細(xì)胞。

圖1 研究人員發(fā)現(xiàn)編碼T細(xì)胞受體的基因在人和人群之間存在很大差異(圖源:[1])
該研究的主要作者Gunilla Karlsson Hedestam說(shuō):“人類TCR基因的變化程度以前是未知的。”
通過(guò)對(duì)血液樣本的深度測(cè)序,研究人員檢測(cè)了來(lái)自撒哈拉以南非洲、東亞、南亞和歐洲的45人的TCR基因。研究人員表明,這些基因在不同的人和人群之間差異很大。這一結(jié)果得到了1000個(gè)基因組計(jì)劃中數(shù)千個(gè)額外病例的分析的證實(shí)。

圖2 45名供體的TRAV基因量
“我們發(fā)現(xiàn),除了同卵雙胞胎,每個(gè)人都有一組獨(dú)特的TCR基因變異。這些差異揭示了我們?cè)谌巳核缴嫌^察到的對(duì)感染和疫苗的廣泛反應(yīng)的可能機(jī)制”。
“我們發(fā)現(xiàn)了175個(gè)新的基因變異,這是已知TCR基因變異數(shù)量的兩倍。一個(gè)意想不到和令人驚訝的發(fā)現(xiàn)是,某些基因變異起源于尼安德特人,其中一種存在于歐洲和亞洲20%的現(xiàn)代人身上。”
Gunilla Karlsson Hedestam解釋說(shuō),這些基因的變異無(wú)法用全基因組測(cè)序中使用的標(biāo)準(zhǔn)方法檢測(cè)到,但隨著專門的深度測(cè)序方法和分析軟件的發(fā)展,可以高度精確地定義B細(xì)胞和t細(xì)胞受體基因,這現(xiàn)在是可能的。
Martin Corcoran說(shuō):“由于這些基因是我們基因組中最易變的基因之一,研究結(jié)果也為我們的免疫系統(tǒng)在歷史進(jìn)程中是如何發(fā)展的提供了新的信息。”我們特別感興趣的是揭示我們從尼安德特人祖先那里遺傳的TCR變體的功能。這些變異在現(xiàn)代人身上的頻率表明,在我們的生物學(xué)中有一種有利的功能,我們渴望了解這一點(diǎn),”馬丁·科克倫補(bǔ)充道。
研究人員現(xiàn)在發(fā)表的這些發(fā)現(xiàn)和新的TCR基因數(shù)據(jù)庫(kù)對(duì)未來(lái)新的治療方法的發(fā)展具有重要意義。

圖3 TCR等位基因的群體差異(圖源:[1])
“了解人類遺傳學(xué)是開發(fā)靶向治療的基礎(chǔ)。研究中描述的方法提供了新的機(jī)會(huì),尤其是在癌癥領(lǐng)域,t細(xì)胞是幾種有前途的免疫治療形式的核心。”Gunilla Karlsson Hedestam說(shuō)。
研究結(jié)果還可以為其他領(lǐng)域的研究提供啟示。
Gunilla Karlsson Hedestam說(shuō):“這些發(fā)現(xiàn)可能導(dǎo)致包括精準(zhǔn)醫(yī)學(xué)在內(nèi)的一系列醫(yī)學(xué)學(xué)科開發(fā)新的診斷和治療方法。”
“我們現(xiàn)在正在研究幾個(gè)新發(fā)現(xiàn)的基因變異的功能意義,以及這種變異如何影響我們的t細(xì)胞反應(yīng)。我們還計(jì)劃進(jìn)行大規(guī)模的個(gè)體研究,以研究TCR基因變異在我們已知的涉及T細(xì)胞的疾病中所起的作用,如傳染病、癌癥和自身免疫性疾病,”Gunilla Karlsson Hedestam說(shuō)。
這些實(shí)驗(yàn)是在麥考瑞Galleria研究機(jī)構(gòu)使用道德的Galleria mellonella(大蠟蛾幼蟲)動(dòng)物模型替代進(jìn)行的,這是澳大利亞第一個(gè)這樣的動(dòng)物模型。
參考資料:
[1] Archaic humans have contributed to large-scale variation in modern human T cell receptor genes. Martin Corcoran, Mark Chernyshev, Marco Mandolesi, Sanjana Narang, Mateusz Kaduk, Kewei Ye, Christopher Sundling, Anna F?rnert, Taras Kreslavsky, Carolina Bernhardsson, Maximilian Larena, Mattias Jakobsson, Gunilla B. Karlsson Hedestam, Immunity, online den 15 februari 2023.



