摘要:研究人員現(xiàn)在能夠在實驗室中指導人類干細胞形成新的血管。
利用計算機設計的蛋白質,研究人員現(xiàn)在已經(jīng)證明,他們能夠在實驗室中指導人類干細胞形成新的血管。再生醫(yī)學的這一里程碑為修復受損的心臟、腎臟和其他器官帶來了新的希望。
華盛頓大學醫(yī)學院的科學家領導了這個項目。他們的研究結果發(fā)表在6月10日的《Cell》雜志上。華盛頓大學醫(yī)學院生物化學資深作者和教授Hannele Ruohola-Baker說:“無論是心臟病、糖尿病還是自然衰老,我們都會在身體組織中累積損傷。修復這種損傷的一種方法可能是在需要恢復健康血液供應的區(qū)域推動新血管的形成。生長因子在組織發(fā)育、傷口愈合和癌癥中起著關鍵作用。通過與細胞外部的受體結合,這些分子驅動細胞內部的變化。幾十年來,研究人員一直試圖將自然生長因子作為再生藥物,取得了一些有限的成功,但由于不精確,許多這些實驗性治療都失敗了。

圖1 NLRC5感知NAD+損耗形成泛視小體并驅動泛視癥和炎癥
“我們開始創(chuàng)造定制的蛋白質,以非常精確的方式與細胞生長因子受體結合。當我們在實驗室制造這些分子并用它們處理人類干細胞時,我們看到不同種類的血管系統(tǒng)的發(fā)育取決于我們使用的蛋白質。這是一個全新的控制水平,”Natasha Edman解釋說,她是這項研究的主要作者,也是華盛頓大學醫(yī)學家培訓計劃的應屆畢業(yè)生。
研究人員用計算機設計了環(huán)狀蛋白質,每個蛋白質針對多達8個成纖維細胞生長因子受體。他們發(fā)現(xiàn),通過改變環(huán)的大小和其他蛋白質特性,他們可以控制干細胞在實驗室條件下的成熟方式。
所得到的血管網(wǎng)功能成熟。它們形成了管子,被劃傷后會愈合,并像預期的那樣從周圍環(huán)境中吸收營養(yǎng)。當移植到老鼠體內時,這些微小的人類血管網(wǎng)在三周內就與動物的循環(huán)系統(tǒng)建立了聯(lián)系。
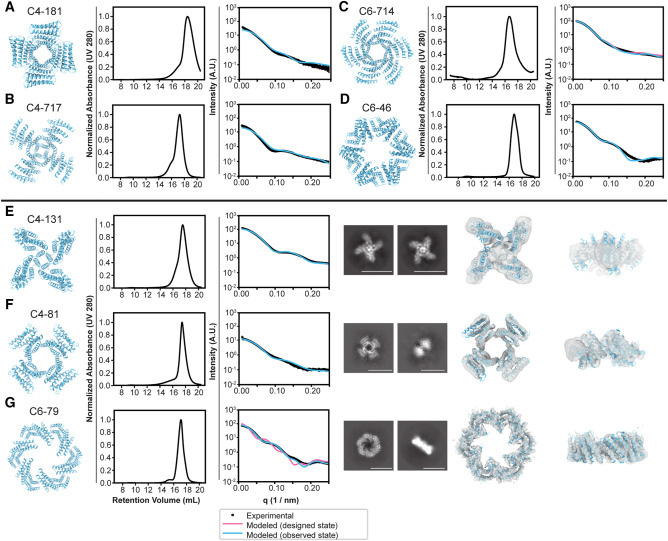
圖2 設計的蛋白質低聚物的生物物理特性
“這項研究表明,可以通過設計創(chuàng)造出具有精致生物功能的定制蛋白質。這將幫助科學家了解生物學,并最終預防和修復疾病,”資深作者David Baker說。
“我們決定先專注于構建血管,但同樣的技術應該適用于許多其他類型的組織。這開辟了研究組織發(fā)育的新途徑,并可能導致一類新的藥物用于脊髓損傷和其他目前沒有好的治療選擇的疾病,”華盛頓大學生物工程博士候選人,該研究的主要作者Ashish Phal說。
這項研究是在華盛頓大學醫(yī)學院蛋白質設計研究所和干細胞與再生醫(yī)學研究所進行的,合作者包括紐約大學醫(yī)學院、德黑蘭醫(yī)科大學、耶魯大學醫(yī)學院、Brotman Baty精密醫(yī)學研究所和Allen發(fā)現(xiàn)細胞譜系追蹤中心。
參考資料
[1] Modulation of FGF pathway signaling and vascular differentiation using designed oligomeric assemblies
摘要:研究人員現(xiàn)在能夠在實驗室中指導人類干細胞形成新的血管。
利用計算機設計的蛋白質,研究人員現(xiàn)在已經(jīng)證明,他們能夠在實驗室中指導人類干細胞形成新的血管。再生醫(yī)學的這一里程碑為修復受損的心臟、腎臟和其他器官帶來了新的希望。
華盛頓大學醫(yī)學院的科學家領導了這個項目。他們的研究結果發(fā)表在6月10日的《Cell》雜志上。華盛頓大學醫(yī)學院生物化學資深作者和教授Hannele Ruohola-Baker說:“無論是心臟病、糖尿病還是自然衰老,我們都會在身體組織中累積損傷。修復這種損傷的一種方法可能是在需要恢復健康血液供應的區(qū)域推動新血管的形成。生長因子在組織發(fā)育、傷口愈合和癌癥中起著關鍵作用。通過與細胞外部的受體結合,這些分子驅動細胞內部的變化。幾十年來,研究人員一直試圖將自然生長因子作為再生藥物,取得了一些有限的成功,但由于不精確,許多這些實驗性治療都失敗了。

圖1 NLRC5感知NAD+損耗形成泛視小體并驅動泛視癥和炎癥
“我們開始創(chuàng)造定制的蛋白質,以非常精確的方式與細胞生長因子受體結合。當我們在實驗室制造這些分子并用它們處理人類干細胞時,我們看到不同種類的血管系統(tǒng)的發(fā)育取決于我們使用的蛋白質。這是一個全新的控制水平,”Natasha Edman解釋說,她是這項研究的主要作者,也是華盛頓大學醫(yī)學家培訓計劃的應屆畢業(yè)生。
研究人員用計算機設計了環(huán)狀蛋白質,每個蛋白質針對多達8個成纖維細胞生長因子受體。他們發(fā)現(xiàn),通過改變環(huán)的大小和其他蛋白質特性,他們可以控制干細胞在實驗室條件下的成熟方式。
所得到的血管網(wǎng)功能成熟。它們形成了管子,被劃傷后會愈合,并像預期的那樣從周圍環(huán)境中吸收營養(yǎng)。當移植到老鼠體內時,這些微小的人類血管網(wǎng)在三周內就與動物的循環(huán)系統(tǒng)建立了聯(lián)系。

圖2 設計的蛋白質低聚物的生物物理特性
“這項研究表明,可以通過設計創(chuàng)造出具有精致生物功能的定制蛋白質。這將幫助科學家了解生物學,并最終預防和修復疾病,”資深作者David Baker說。
“我們決定先專注于構建血管,但同樣的技術應該適用于許多其他類型的組織。這開辟了研究組織發(fā)育的新途徑,并可能導致一類新的藥物用于脊髓損傷和其他目前沒有好的治療選擇的疾病,”華盛頓大學生物工程博士候選人,該研究的主要作者Ashish Phal說。
這項研究是在華盛頓大學醫(yī)學院蛋白質設計研究所和干細胞與再生醫(yī)學研究所進行的,合作者包括紐約大學醫(yī)學院、德黑蘭醫(yī)科大學、耶魯大學醫(yī)學院、Brotman Baty精密醫(yī)學研究所和Allen發(fā)現(xiàn)細胞譜系追蹤中心。
參考資料
[1] Modulation of FGF pathway signaling and vascular differentiation using designed oligomeric assemblies



